VITA 1600 Bulevar de Wilson, Apartamento 500, Arlington, Virgínia 22209 E.U.A. TEL: 703/276-1800. Fac-símile: 703/243-1865 Internet: pr-info@vita.org
Understanding Baterias ISBN: 0-86619-225-5 [C]1985, Voluntários em Ajuda Técnica,
PREFACE
Este papel é um de uma série publicada por Voluntários dentro Técnico Ajuda para prover uma introduçăo a estado-de-o-arte específica tecnologias de interesse para pessoas em países em desenvolvimento. É pretendida que os documentos săo usados como diretrizes para ajudar pessoas escolhem tecnologias que săo satisfatório ŕs situaçőes deles/delas. Năo é pretendida que eles provęem construçăo ou implementaçăo săo urgidas para as Pessoas de details. que contatem VITA ou uma organizaçăo semelhante para informaçăo adicional e ajuda técnica se eles achado que uma tecnologia particular parece satisfazer as necessidades deles/delas.
Foram escritos os documentos na série, foram revisados, e foram ilustrados quase completamente por VITA Volunteer os peritos técnicos em um puramente basis. voluntário Uns 500 voluntários eram envolvidos na produçăo dos primeiros 100 títulos emitidos, enquanto contribuindo aproximadamente 5,000 horas do time. deles/delas o pessoal de VITA incluiu Maria Giannuzzi como editor, Suzanne Brooks que controla typesetting e plano, e Margaret Crouch como gerente de projeto.
O autor deste papel, VITA Horace McCracken Voluntário, é o presidente do McCracken Companhia Solar em Alturas, Califórnia. O co-autor, VITA Joel Gordes Voluntário, é atualmente o solar projete o analista para o Estado da Hipoteca Solar de Connecticut Subsídio Program. Os revisores também săo o VITA volunteers. Daniel Dunham fez consultando em fontes solares e alternativas de energia para VITA e AID. Ele viveu e trabalhou em Índia, Paquistăo, e Morocco. que Sr. Dunham também preparou para uma estado-de-o-arte inspecione em silęncios solares para AJUDA. Jacques Le Normand é Assistente Diretor no Instituto de Pesquisa de Cinta, Quebec, Canadá, que pesquisa em energia renovável. Ele supervisionou trabalho com coletores solares e escreveu vários publiations em solar e energia de vento, e conservaçăo. DARRELL G. Phippen é um + engenheiro mecânico e especialista de desenvolvimento com que trabalham Comida para o Faminto em Scottsdale, Arizona.
VITA é uma organizaçăo privada, sem lucro que apóia as pessoas trabalhando em problemas técnicos em países em desenvolvimento. ofertas de VITA informaçăo e ajuda apontaram a ajudar os indivíduos e grupos para selecionar e tecnologias de instrumento destinam o deles/delas situations. VITA mantém um Serviço de Investigaçăo internacional, um centro de documentaçăo especializado, e uma lista computadorizada de voluntário os consultores técnicos; administra projetos de campo a longo prazo; e publica uma variedade de manuais técnicos e documentos.
I. INTRODUÇĂO DE
Baterias foram em uso por muitos anos, mas hoje há um maior demanda para poder de bateria que já antes de. que Isto renovou interesse năo só foi provocado por desenvolvimentos novos mas também pela diversidade de usos para baterias em civil, industrial, e aplicaçőes militares.
Este papel provę uma compreensăo básica de baterias e rastros + desenvolvimento deles/delas dos cedo 1800s para a Pesquisa de day. presente e desenvolvimento continua em um esforço para resolver o inerente isto é, fraqueza de baterias como empacotar mais energia em um pacote menor.
Uma cela elétrica ou bateria é um dispositivo que transforma o energia química conteve diretamente dentro de seus materiais ativos em energia elétrica por meio de uma reaçăo de electrochemical. Este tipo de reaçăo envolve a transferęncia de elétrons de um material para outra por uma soluçăo administrando. Historically, baterias fizeram um papel importante nos dias cedo de elétrico desenvolvimento ambos nos Estados Unidos e na Europa.
Em 1800 nomeado um cientista italiano Volta descobriu isso por dois condutores dissimilares imergindo em uma soluçăo química um electromotive forçam (EMF) ou voltagem era estabelecida entre o dois conductors. Figure 1 ilustra uma cela de Voltaic simples.
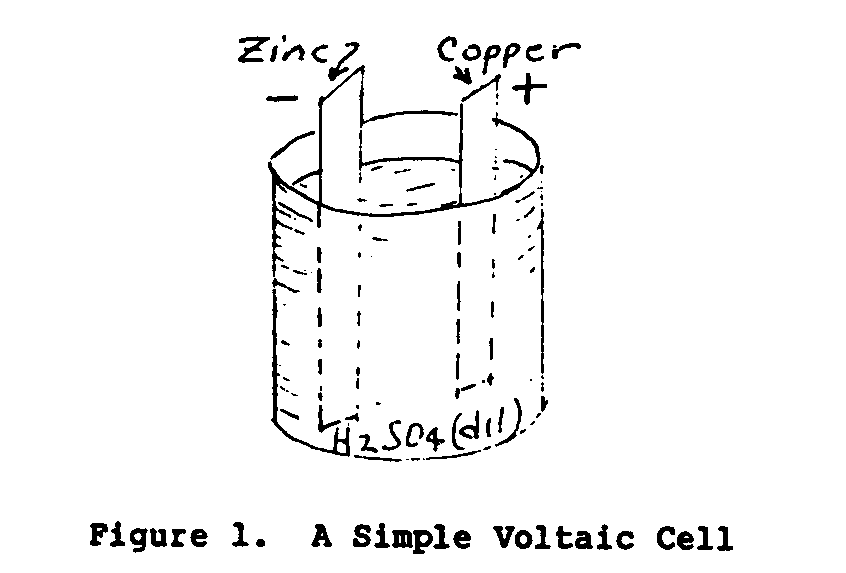
Săo chamados os condutores sólidos da cela elétrodo e o líquido administrando o eletrólito. que UMA cela consiste em dois elétrodo e um electrolyte. UMA bateria consiste em um ou mais cells. A voltagem da cela depende no material do elétrodo e o eletrólito. A produçăo atual elétrica e + poder da cela é dependente nas dimensőes de prato e + peso do material de elétrodo.
Há dois tipos gerais de baterias em uso hoje: o primário tipo ou " cela " seca e o armazenamento secundário battery. UM bateria primária produz uma corrente por açăo de descarga quando um dos elétrodo da cela é decomposta durante uso. Este tipo de cela năo podem ser restabelecidas usar novamente recarregando e o cela inteira deve ser descartada quando năo for nenhum active. Secondary mais longo por outro lado, celas săo quimicamente reversíveis e lata seja carregada e descarregou durante muitos ciclos de operaçăo antes sendo substituída.
Na cela de voltagem simples mostrada em Figura 2, quando dois dissimilar metais, zinco e cobre, estăo suspensos em um eletrólito de dilua ácido sulfúrico, um potencial de approxiamtely 1.10 volts exista entre os elétrodo. que O elétrodo de zinco será negativo e o elétrodo de cobre será positivo. Quando o troque no circuito de carga externo está fechado, um testamento atual, flua pela carga (energia-absorvendo dispositivo) e bateria em acordo para a Lei de Ohm. (*) Como a corrente de carga continua fluindo, hidrogęnio como bolhas se aparecerá e cobrirá o cobre chapeou, e + prato de zinco dissolverá gradualmente. A desvantagem principal com esta cela é que o gás borbulha aumento o interno resistęncia da cela, fazendo produçăo atual diminuir.
* A corrente direta que flui em um circuito elétrico é diretamente proporcional ŕ voltagem aplicada ao circuito. A constante de proporcionalidade R, chamou a resistęncia elétrica, é determinado pela equaçăo V = RI no qual " V " é a voltagem aplicada e Eu " sou a corrente.
II. VARIAÇŐES DE TECNOLOGIA
BATERIAS PRIMÁRIAS
Vários tipos diferentes de primário-tipo molharam foram desenvolvidas celas e usado nos Estados Unidos. Celebridade de Most entre estes seja o cela de gravidade, a cela de óxido de cáustico-cobre, o ar-depolarized cela, e a cela de Lelanche. Cada cela teve seu próprio operando características, e capacidades atuais variaram de menos que um ampčre (ampčre) para a cela de Lelanche para vários cem ampčres para a cela de óxido de cáustico-cobre. que A agęncia postal britânica desenvolveu uma cela molhada conhecida como a cela do Daniel que ofereceu vários características operacionais excelentes.
Havia duas dificuldades principais com a cela de primário-tipo construçăo, deterioraçăo por açăo local e polarizaçăo de cela. Açăo local é uma açăo química interna inerente para baterias; a vida da cela é diminuída gradualmente até mesmo entretanto nenhuma carga é conectada a seus términos. que açăo Local é definida como a descarga de material ativo de qualquer um prato devido para um pouco de impureza no eletrólito ou material de prato. Isto açăo causa a formaçăo de celas dadas curto circuito que causam + metal para deteriorar.
Polarizaçăo de cela é causada por bolhas de hidrogęnio que săo depositadas no cátodo quando fluxos atuais pela cela. que Isto abaixa a voltagem terminal e aumentos a resistęncia interna do battery. métodos Vários por neutralizar este efeito polarizando era usado, ou por substância química ou construçăo mecânica que conduzida ao desenvolvimento do ar-depolarized cela.
No ar-depolarized cela, o elétrodo foi feita de um altamente forma absorvente de carbono e estava suspenso sobre o eletrólito level. desde que o elétrodo de carbono năo foi imergida no eletrólito soluçăo, polarizaçăo da cela foi prevenida. Em operaçăo, oxigęnio que cerca a superfície porosa do carbono, elétrodo combina com o hidrogęnio evoluiu ŕ superfície de + elétrodo de carbono e eletrólito. que ventilaçăo Bom foi requerido manter uma provisăo de ar satisfatória para operaçăo. O Edison carbono cela e a bateria de Carbonaire eram representativas do ar-depolarized tipo. Wet que celas de primário-tipo tęm em grande parte substituída pela bateria de armazenamento de secundário-tipo.
O dia " moderno cela seca " que foi desenvolvida por Georges Lelanche em 1868, é uma modificaçăo do Lelanche velho molhou cela. A diferença é isso só água suficiente é somada o eletrólito para umedecer um forro absorvente. A cela seca moderna é o amplamente usado de todas as baterias primárias hoje principalmente por causa do baixo custo deles/delas, desempenho seguro, e difundido availability. que săo feitas baterias de cela Secas em avaliaçőes de 1.5, 3, 6, 7.5, 9, 22.5, 45, 67, e 90 volts.
O tipo mais comum de construçăo para uma cela seca é mostrado dentro Figure 3.

A cela em Figura 3 usos uma vara de carbono para o ânodo ou positivo terminal e um recipiente de zinco externo (caso) para o negativo terminal. O caso de zinco tem um forro interno de papel absorvente material que é saturado com o eletrólito. O espaço entre os elétrodo está cheio com uma mistura de coca-cola esmagada, dioxide de manganęs, e grafita. Manganęs de é somado como um depolarizer. O eletrólito é salammonic e cloreto de zinco. O topo do caso é lacrado com uma combinaçăo marcando e o zinco recipiente é incluso em um recipiente de papel. A voltagem de um novo cela seca é 1.4 a 1.6 volts.
Baterias de cela secas entram em tręs classes gerais: (1) lanterna baterias normalmente 1-1/4 polegada em diâmetro e 2-1/2 polegadas alto com uma capacidade atual de cerca de 3 ampčre-horas; (2) tamanho grande celas, mais geralmente chamado o Número 6 cela seca, aproximadamente, 2-1/2 polegadas em diâmetro e 6 polegadas alto com um avaliaçăo atual de cerca de 30 ampčre-horas; e (3) o " industrial " e voltagem alta digita que poderia ser uma cela ou uma combinaçăo de celas, usado em serviço industrial com capacidades atuais de 50 ampčre-horas ou greater. A capacidade de ampčre-hora é a taxa de descarregue uma bateria pode manter para um determinado período de tempo, normalmente oito hours. por exemplo, uma 30 ampčre-hora taxou bateria normalmente possa prover aproximadamente 3-1/2 ampčres durante oito horas. Como ordinariamente porém, celas secas usadas provęem menos que a avaliaçăo deles/delas. A vida de prateleira está limitada por açăo local e por isso alguns fabricantes estampam uma data de serviço na coberta exterior de cada cell. açăo Local causa deterioraçăo eventual do bateria, e depois de aproximadamente um ou dois armazenamento de anos, a bateria se torna useless. desde que o elétrodo de zinco forma parte do exterior parede, sua destruiçăo gradual debilita a estrutura de cela, e como + gás de hidrogęnio desenvolvido constrói pressăo interna, pode rompa e derrame seus conteúdos corrosivos. por isto, equipamento nunca deveria ser armazenada com celas secas em cima de períodos longos de time. celas Secas năo requerem nenhuma manutençăo e quando eles nenhum mais longo opere está descartado e substituída.
Um mais recente tipo de cela seca desenvolvido é o Ruben ou Mercúrio cela (Figura 4) . pelo que Esta cela foi desenvolvida durante Segunda Guerra Mundial
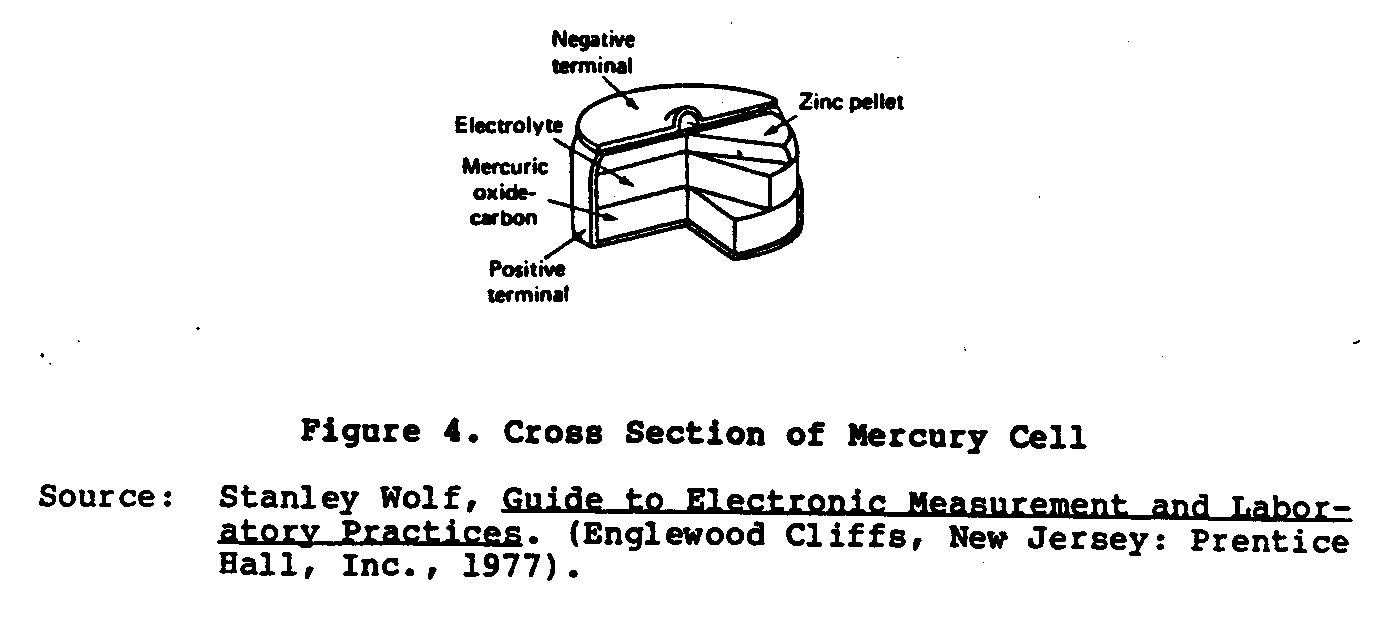
Ruben Laboratories e P.R. Companhia de Mallory por operar pequeno equipamento eletrônico que requer poder atual alto. que Esta cela é feita em duas formas: o " ânodo " de rolo e o " botăo digitam. " O ânodo é amalgamado zinco e o cátodo é um óxido mercurial material de depolarized misturou com grafita. O eletrólito é um soluçăo de hydroxide de potássio (KOH) contendo zincate de potássio. Estas celas săo longe superiores ao Lelanche cela devendo seco para o tamanho compacto deles/delas, característica de voltagem plana, e muito tempo estante life. A voltagem de nenhum-carga destas celas é 1.34 volts.
Foram feitos vários desenvolvimentos avançados em baterias pequenas, ambos primário e celas de secundário-tipo que incluem o magnésio, alcalino, prata-zinco, e lithium. Mesa de 1 listas o

características e aplicaçőes destas celas.
BATERIAS DE ARMAZENAMENTO SECUNDÁRIAS
Desde 1965, houve interesse renovado usando armazenamento baterias em poder systems. que Isto é porque consumo de poder moderno envolve demandas de carga muito desiguais e carga de cume crescente demands. Quando um sistema tem que entregar mais poder (aumento em carga demanda), o provedor pode conhecer a demanda por qualquer um trocando um gerador adicional sobre o sistema ou trocando um carregou banco de bateria sobre o line. O posterior requer um muito menor investimento.
O revivificaçăo de baterias como poder unidades de sistema tęm principalmente começada com sistemas independentes pequenos como vento - ou água-dirigida generators. Em tais sistemas, baterias de armazenamento executam dois functions. First importante, durante períodos de baixa demanda de carga, a bateria de sistema pode armazenar muito da energia gerada, que seria perdida caso contrário ao sistema. Second, energia, armazenada durante o período de fora-cume está disponível durante tempos de carga de cume demand. A importância do posterior pode ser ilustrada com o exemplo quantitativo seguinte: Suponha o capacidade da bateria tem uma taxa de poder de descarga igual para meio da capacidade de poder de gerador ([P.sub.B] = 0.5 [P.sub.G]) . Isto significa isso debaixo de condiçőes normais, durante períodos de demanda de carga alta, o combinaçăo de gerador-bateria pode durante várias horas sirva uma carga de até 1.5 vezes isso que o gerador só poderia servir.
Outra razăo para o interesse aumentado em armazenamento secundário baterias săo a necessidade por poder de auxilio por alguns do mais novo technology. por exemplo, mais mais dos computadores modernos envolva alguma forma de " armazenamento volátil " de informaçăo, é isso, a informaçăo é perdeu se poder é removed. para vigiar contra esta possibilidade, muitos, sistemas de computador usam " uninterruptible " dăo poder a sistemas, baseado em baterias de armazenamento, prover corrente elétrica ao computador, equipamento quando poder comercial está perdido.
A bateria de armazenamento, construída com celas molhadas secundárias, é semelhante em açăo para uma cela primária, exclua as açőes químicas envolvida é praticamente completamente reversível. Once que a cela é descarregada, atual de uma fonte externa, atravessou o cela na direçăo oposta, restabelecerá substancialmente o bateria para seu original carregou condiçăo.
Há tręs tipos de baterias de armazenamento atualmente disponível: (1) o tipo de conduzir-ácido; (2) o níquel-ferro ou bateria alcalina (Cela de Edison); e (3) o níquel-cádmio ou álcali-tipo (Nicad).
Baterias de conduzir-ácido
A bateria de conduzir-ácido é o amplamente tipo usado de bateria hoje por causa de seu baixo custo, confiança, desempenho bom, características, e aplicaçăo larga. que Esta bateria é fabricada em muitos tamanhos e capacidades que variam de 1 ampčre-hora até várias mil ampčre-horas que taxam. *
A cela de armazenamento usa reactive esfregam dianteira para o negativo elétrodo (Pb), conduza dioxide para o elétrodo positivo (Pb0), e dilui ácido sulfúrico para o eletrólito. O elétrodo materiais tęm pouca força estrutural e devem ser apoiados em pratos ou grids. A grade do prato de bateria tem duas funçőes: primeiro, apóia o material de prato ativo; e segundo, serve como um condutor conectar o prato terminal para tudo partes do material ativo.
Conduza pratos de bateria de armazenamento săo divididos em dois tipos, o Plante (formou) e o Faure (colou), como mostrada em Figura 5. Dentro + Plante-tipo de construçăo que o material ativo é eletricamente formada de pura dianteira por um processo de electrochemical do dianteira metálica da grade apoiando. No Faure-tipo o material ativo é aplicado ŕ grade apoiando na forma de um follwed de pasta por uma colocaçăo, secando, e formando operaçăo.
Figure 5 espetáculos o Plante (UM) e Faure (B) conduza cela plates. O săo soldadas assembléias de cela junto para formar positivo e negativo grupos que săo intercalados folhas em branco para fazer as pazes junto o completo bateria que săo colocadas Separador de cell. entre os elétrodo, e o elemento completo é colocado em um recipiente e sealed. O uso de pratos grandes com limites de espaçamento íntimos a resistęncia interna da bateria para um baixo nível. Figure 6 espetáculos um cortante

visăo da cela de armazenamento de dianteira.
Durante descarga é convertido o material de bateria de ambos os pratos em dianteira sulfate. A quantia de sulfate de dianteira formou pratos de onthe e a quantia de ácido perdeu do eletrólito é dentro exato proporcione ŕ taxa de descarga. Os objetos pegados de açăo inversos lugar quando a cela é carregada. Cela de que reaçőes químicas săo representada pela equaçăo seguinte; porém, isto é um forma simplificada como a açăo atual é complicada muito mais.
* Bateria ampčre-hora taxar normalmente é baseado em uma descarga de 8-hora taxa.
Ao prato positivo:
PB[O.SUB.2] + HS[O.SUB.4][SUP. -] + [3H.SUP.+] + [2E.SUP. -] (*)-----> PB[SO.SUB.4] + 2[H.SUB.2]O
Ao prato negativo:
Pb + HS[O.sub.4][sup. -]-----> Pb[SO.sub.4] + [H.sup.+] + [2e.sup. -]
A reaçăo de cela combinada para descarga e custo é expressado pela equaçăo seguinte:
descarregam -------------> Pb[O.sub.2] + Pb + 2[H.sub.2] S[O.sub.4] <= == == = 2Pb[SO.sub.4] + 2[H.sub.2]O + energia elétrica sulfúrico plate de plate pratos de ácidos <-------------; carregam
Em descarga o ácido separa do eletrólito e formas um combinaçăo química com os pratos, mudando isto para conduzir sulfate. Como continua descarga, ácido adicional é tirado do eletrólito até que atual deixará de fluir. A água, formou pela perda de ácido para os pratos, abaixa o permanecendo específico gravidade (* *) do eletrólito. em comum prática, descarga é sempre parada antes dos pratos tenha sulfated completamente, porque uma vez completamente sulfated, condiçăo de bateria năo pode ser convertida atrás para material ativo em custo. Em custo a açăo inversa objetos pegados colocam: o ácido nos pratos de sulfated é dirigido atrás em + eletrólito, e o S[O.sub.4] combina com hidrogęnio na água formar ácido sulfúrico adicional ([H.sub.2][SO.sub.4]).
Eletrólito para celas de conduzir-ácido é diluir acid. sulfúrico Para um bateria completamente carregada para a que a gravidade específica varia de 1.200 1.30 e quando descarregou 1.150 (pura água mede 1.00) . O gravidade específica está medida por um hidrômetro de seringa-tipo como mostrada em Figura 7, e valores săo temperatura corrigida.
* O símbolo e - representa elétrons.
* * Gravidade específica está definida como a relaçăo de peso de um determinado volume de uma substância para um volume igual de pura água. A voltagem de uma cela de dianteira é aproximadamente 2.10 volts a nenhuma carga mas é mais alto ao ser carregada. voltagem Normal em custo é 2.15 volts e como a cela chega custo cheio este valor rapidamente aumentos para entre 2.5 e 2.6 volts. Este intervalo posterior de custo é conhecido como o " período " de gassing. Gassing do eletrólito a qualquer hora durante carregar deveria ser evitada como o taxa de custo também é high. Como uma cela alcança seu final completamente condiçăo carregada, uma corrente alta năo é aconselhável como este excesso corrente decompőe a água no eletrólito que é dirigida fora na forma de gás.
A bateria de conduzir-ácido tem várias desvantagens: (1) celas săo temperatura sensível e perde poder em temperaturas frias; (2) pratos de cela tendem a afivelar e torcer em corrente contínua, alta conserte, e (3) cuidado especial deve ser observado quando uma bateria for năo usada para períodos longos, caso contrário as celas văo sulfate.
Baterias de níquel-ferro
O níquel-ferro ou bateria alcalina foram desenvolvidas para superar o desvantagens inerentes da cela de conduzir-prato. é um radical partida disto em construçăo e operaçăo. No Estados Unidos esta bateria é conhecida como a " cela de Edison, " nomeou depois de seu inventor Thomas UM. Edison. Figure 8 espetáculos a construçăo

de um cell. típico O prato positivo consiste em aço tubos que contęm hidrato de níquel e níquel somaram em substituto layers. O prato negativo é formado de caixas de aço planas ou bolsos que estăo picotado e acumulado com grânulos de óxido férreos. Grades de folha-aço apóiam estes tubos e bolsos que săo fugida para formar cela positiva e negativa Cela de groups. junto términos e o recipiente de aço săo níquel chapeado. Todos os separador e săo feitas partes isolantes de borracha. A cela usa um eletrólito de 21 soluçăo de por cento de potassa cáustica que contém um quantia pequena de hidrato de lithium.
A química desta cela é bastante complicada, e a substância química reaçăo que acontece dentro da cela é completamente diferente de + da dianteira cell. que O eletrólito somente age como um administrando médio e năo entra em combinaçăo com qualquer do material de prato ativo durante operaçăo. Sua gravidade específica restos praticamente constante durante o ciclo completo de custo e discharge. Condition de custo de bateria ou descarga é determinado por um voltmeter que lę e năo pela gravidade específica de + electrolyte. que A reaçăo de cela de bateria alcalina é:
descarregam ------------------>
[Fe.sub.2] + 2NiOOH + KOH + 2[H.sub.2]O-------> [Fe.sub.2][(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elétrico <------;
<-----------------; energia de
CHARGE
A voltagem de cada cela é aproximadamente 1.50 volts em aberto circuito, mas é mais alto em custo e abaixa debaixo de condiçőes de carga. Estas baterias săo determinadas um ampčre-hora capacidade taxando fundou na taxa deles/delas de descarga até a voltagem final de 1.00 por cell. Algumas avaliaçőes atuais săo baseadas em uma 5-1/2-hora contínuo taxa de descarga, enquanto outros săo baseados em uma taxa de 3-1/2-hora.
Ao contrário a bateria de conduzir-cela, năo há nenhuma voltagem mínima abaixo + qual este tipo de cela năo pode ser descarregado. na realidade, esta cela pode ser descarregada zerar volts, dada curto circuito a seus términos, e partiu nesta condiçăo para um período indefinido. Isto é o método pelo qual uma bateria alcalina é posta em armazenamento.
Também, esta cela pode ser cobrada demais acidentalmente, carregou dentro o direçăo errada, e momentaneamente deu curto circuito sem dano. Baterias alcalinas năo estăo feridas gelando e um eletrólito com uma gravidade específica de 1.200 ŕs 15.5[degrees]C (60[degrees]F) gela sólido ŕs -66[degrees]C (-87[degrees]F). que O eletrólito desta cela deteriora gradualmente durante uso e deve ser mudada eventualmente.
As vantagens principais da cela de níquel-ferro săo: (1) é extremamente luz e forte devido a sua construçăo de aço; (2) oferece uma vida indefinidamente longa; e (3) supera o problema de sulfating de cela da bateria de conduzir-ácido. O chefe desvantagem é seu alto primeiro custo e resistęncia interna alta.
Baterias de níquel-cádmio
Níquel-cádmio ou baterias de Nicad, uma adiçăo relativamente nova para celas de armazenamento, foi desenvolvida na Europa. que Estas baterias consistem de intercalou folhas em branco assembléias de positivo e pratos negativos montadas em um recipiente de aço lacrado. O material ativo positivo, níquel, hydroxide, e o material ativo negativo, óxido de cádmio, é encaixada em bolsos de aço idęnticos, finamente perfurados. Os pratos é composta de filas destes bolsos que săo encrespados e formada em aço frames. assembléias de prato Positivas e negativas é trancada junto a barras de ônibus de aço pesadas. Plate que grupos săo intercalada folhas em branco e separou através de varas de plástico magras. A cela elétrico términos e caso săo níquel chapeado. O eletrólito é um soluçăo de potassa cáustica especialmente purificada (hydroxide de potássio) dissolvida em água destilada. Figure 9 espetáculos uma visăo cortante
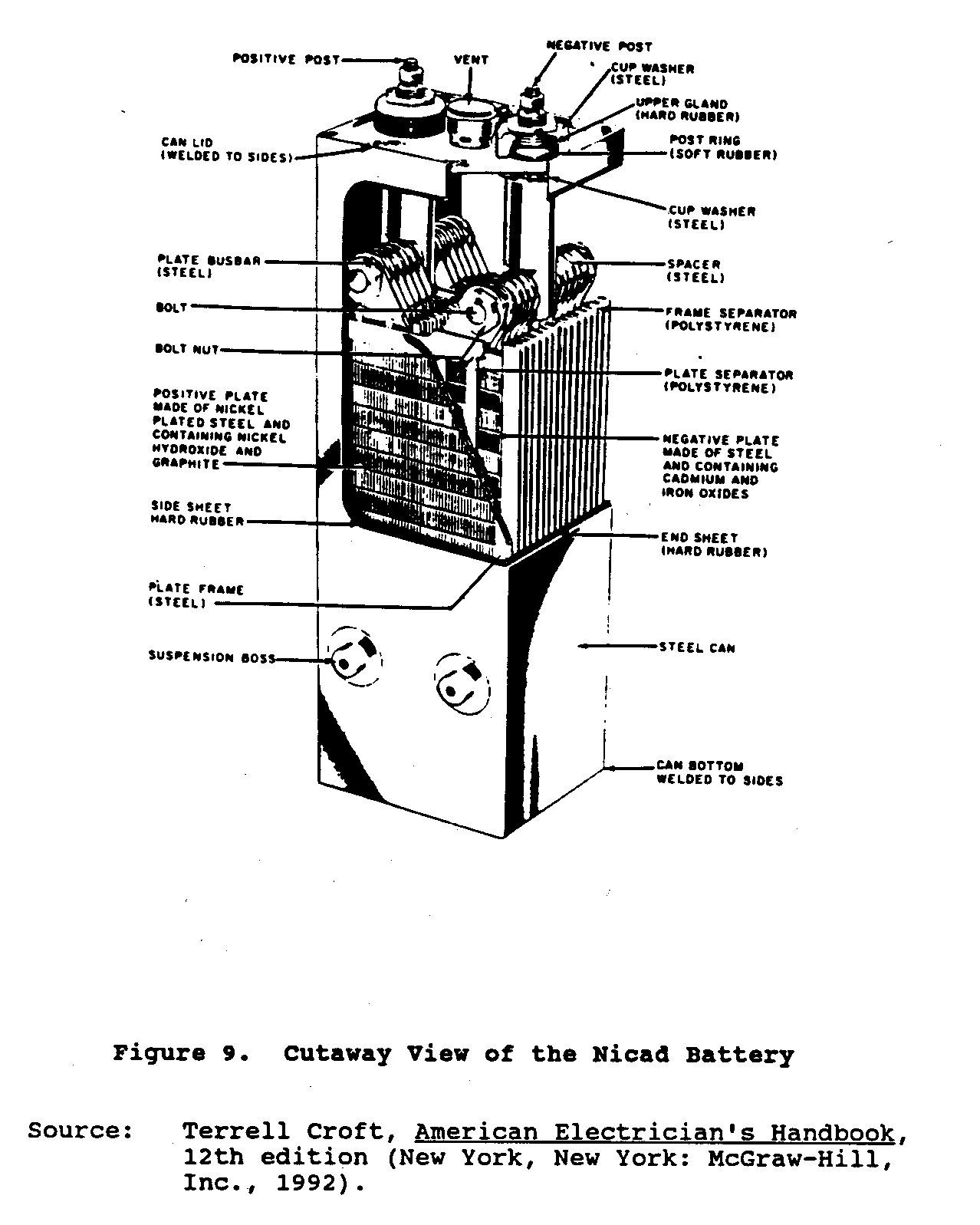
da bateria de Nicad.
A reaçăo de cela simplificada é:
carregam <-------------------;
Cd + 2NIOOH + KOH + 2[H.sub.2]O------> Cd[(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elétrico <------energia; de
-------------------->
descarregam
Durante custo ou descarga da cela, há praticamente năo mude na gravidade específica do eletrólito. Like o Cela de Edison, a funçăo exclusiva do eletrólito é agir como um condutor para a transferęncia de íones de hidrogęnio de um elétrodo para + other. A voltagem que taxa de cada cela é 1.20 volts em aberto circuito; quando conectado a uma carga externa, permanece esta voltagem razoavelmente constante até aproximadamente 90 por cento de seu avaliado capacity. A ampčre-hora que taxa das celas de Nicad é baseada em um voltagem de descarga final de 1.10 volts por cela. Edison Distinto celas, baterias de Nicad serăo danificadas em cima de-descarregando repetido debaixo da cela mínima deles/delas taxando de 1.10 volts. baterias de Nicad tenha uma temperatura gama operacional de -51[degrees]C (-60[degrees]F) para 93[degrees]C (200[degrees]F).
Baterias de Nicad săo vibraçăo e choque resistente devido ao deles/delas acere construçăo; segure bem o custo deles/delas durante longo inativo períodos; mantenha uma fonte de voltagem constante durante descarga; e năo é estragado por cobre demais. no que Estas baterias podem ser montadas qualquer posiçăo em discharge. Como a cela de Edison, a bateria de Nicad tem um alto primeiro custo como comparada com a bateria de conduzir-ácido; porém, este custo alto é compensado pela vida mais longa deles/delas span. UMA comparaçăo de conduzir-ácido, alcalino, e baterias de Nicad săo apresentada em Mesa 2.
Mesa 2. Comparaçăo de Conduzir-ácido, Níquel-ferro, e Baterias de Níquel-cádmio
Operating Cela Vida Typical Temperatura Energia de Custo de / Cell Gama Densidade de Discharge Custo TYPE VOLTAGE ([DEGREES]C) (WH (*) /KG) (CYCLES) ($/WH (*))
Conduzir-Acid 2.0 20 a 30 37 1200-1500 .08 Níquel-Iron 1.2 2.2 a 46 29 Níquel-Cadmium 1.25 (-51) para 93 33
* Watt-horas
Procedimentos de Manutençăo gerais para Baterias de Armazenamento
Própria manutençăo é essencial para serviço sem-defeitos continuado de armazenamento batteries. Enquanto a construçăo de cela é diferente para os vários tipos, manutençăo é semelhante para todos os tipos e consiste nos procedimentos gerais seguintes:
1. Keep celas limpam e secam;
2. Check nível de eletrólito regularmente;
3. Keep baterias carregaram a toda hora; e
4. Keep impurezas de todos os tipos fora de celas como văo eles tęm um efeito prejudicial e eventualmente ruína them. Never usam qualquer ferramenta ou utensílios (hidrômetros, funis, etc.) que foi usado para consertar outros eletrólito diferente disso requerida para aquela bateria específica, especialmente ferramentas usaram para baterias de conduzir-ácido.
5. Refer para as recomendaçőes de fabricantes e mantém um escrito registro de manutençăo.
O eletrólito da cela de conduzir-ácido nunca requer substituiçăo com exceçăo de perda devido a derramamentos acidentais. However, no Edison, e celas de Nicad há um deterioraçăo gradual do eletrólito deles/delas, que deve ser substituída eventualmente em cima da vida do bateria.
BIBLIOGRAPHY/SUGGESTED READING LISTA
BAUMEISTER, T., ED. O Manual de Padrăo de Mark para Engenheiros Mecânicos. 7Ş Ediçăo. Nova Iorque, Nova Iorque,: Livro de McGraw-colina Companhia de , 1967.
CARR, C.C. O Eletricista americano de arte Manual. 8Ş Ediçăo. Nova Iorque, Nova Iorque,: Companhia de Livro de McGraw-colina, 1961.
Fink e Batey. Manual Standard para Engenheiros Elétricos. 11ş Ediçăo de . Nova Iorque, Nova Iorque,: Companhia de Livro de McGraw-colina, 1978.
Hubert, Charles I. Preventative Manutençăo de Equipamento Elétrico. Nova Iorque, Nova Iorque,: Companhia de Livro de McGraw-colina, 1969.
Knowlton, A.E., Manual Standard para Engenheiros Elétricos. 8ş Ediçăo de . Nova Iorque, Nova Iorque,: Companhia de Livro de McGraw-colina, 1949.
Enciclopédia de McGraw-colina de Cięncia e Tecnologia. 5Ş Ediçăo. Nova Iorque, Nova Iorque,: Companhia de Livro de McGraw-colina, 1982.
Timbre e Princípios de Bush. de Engenharia Elétrica. 3Ş Ediçăo. Nova Iorque, Nova Iorque,: Wiley e Filhos, Inc., 1946.
Lobo, Stanley. Guide para Medida Eletrônica e Laboratório, Practices. Precipícios de Englewood, Nova Jersey,: Corredor de Prentice, Inc., 1977.